|
|

 |
|
Межотраслевая Интернет-система поиска и синтеза физических принципов действия преобразователей энергии
|
Общий каталог эффектов
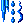 | Сублимация |
 |
Переход из кристаллического состояния в газообразное с поглощением теплоты и увеличением удельного объема
Анимация
Описание
Сублимация (от лат. sublimo – возношу), переход вещества из твердого в газообразное состояние, минуя стадию жидкости (фазовый переход первого рода). Для сублимации к веществу необходимо подвести энергию, называемую теплотой сублимации. Теплота сублимации – количество теплоты, которое необходимо сообщить твердому телу.
Известны природные сублимационно-десублимационные процессы, например: образование газовых гидратов, образование и изменение ядер комет, десублимация водяного пара в атмосфере, сублимация льда.
В случае сублимации при подводе энергии (конвективный или контактный нагрев, нагрев излучением, например лазерным) происходит разрыв межмолекулярныз связей.
Сублимированные вещества могут быть конечными продуктами или направляться на десублимацию, перед которой могут подвергаться промежуточной обработке, например адсорбционной очистке.
При десублимации (процесс самоорганизации) возникают ван-дер-ваальсовы связи между отдельными молекулами вещества с выделением энергии, к-рую отводят от десублимата непосредственно контактом его с охлаждаемой твердой поверхностью, взаимодействием с вводимым дополнительно хладагентом, испарением жидкости (напр., воды), добавляемой в газовую смесь, ее расширением.
Сорбционно-десорбционные процессы, как и другие процессы с фазовыми переходами первого рода, удобно представлять с помощью трехфазной диаграммы состояния (рис. 2). На этой диаграмме сублимационный процесс изображен пунктирными линиями, пересекающими кривую с в точке ниже тройной точки Тр при повышении температуры и постоянном давлении либо при понижении давления и постоянной температуре.
Фазовая диаграмма для сублимационо-десублимационных процессов: а, b, с - кривые давления пара соответственно при плавлении в-ва, над жидкостью, над твердой фазой, Тр-тройная точка; p-давление; T-абсолютная температура.
Рис. 2.
При десублимации переход от гомогенной системы к гетерогенной начинается с образования единичных элементов новой фазы - твердых зародышей (кластеров), которые после достижения критического размера имеют тенденцию к неограниченному росту. Энергия кластеров увеличивается с возрастанием числа входящих в них молекул, стремясь асимптотически к пределу, равному теплоте фазового перехода.
Кинетика сублимации - многостадийный процесс, для проведения которого необходима дополнительная тепловая энергия. При ее подводе частицы вещества мигрируют на поверхности твердой фазы из состояния с наибольшей прочностью связей в состояние с их меньшей прочностью, а затем в газовую фазу. Одновременно из нее происходит десублимация частиц.
Скорости сублимации и десублимации обусловливаются прежде всего скоростью разрушения кристаллов при сублимации и скоростью кристаллизации при десублимации, а также скоростями переноса массы от поверхности твердой фазы в газовый поток. По мере протекания сублимации и десублимации изменяются характеристики твердой фазы (толщина и пористость слоя, шероховатость поверхности и др.) и соответсвенно интенсивность тепло- и массообмена с газовой фазой.
Ключевые слова
Разделы наук
Применение эффекта
Сублимация йода. Возгонка характерна, например, для элементарного йода I2, который при нормальных условиях не имеет жидкой фазы: чёрные с голубым отливом кристаллы сразу превращаются (сублимируются) в газообразный молекулярный йод (медицинский “йод” представляет собой спиртовой раствор).
Известным примером десублимации является появление инея на ветках во время усиления мороза.
Хорошо поддается возгонке также и вода, что определило широкое применение данного процесса как одного из способов сушки. При промышленной возгонке сначала производят заморозку исходного тела, а затем помещают его в вакуумную или заполненную инертными газами камеру. Физически процесс возгонки продолжается до тех пор, пока концентрация водяных паров в камере не достигнет нормального для данной температуры уровня, в связи с чем избыточные водяные пары постоянно откачивают. Возгонка применяется в химической промышленности, в частности, на производствах взрывоопасных или взрывчатых веществ, получаемых осаждением из водных растворов.
На эффекте возгонки основан один из способов очистки твердых веществ. При определенной температуре одно из веществ в смеси возгоняется, а другое нет. Пары очищаемого вещества конденсируют на охлаждаемой поверхности. Прибор, применяемый для этого способа, очистки называется сублиматор.
Возгонка также используется в пищевой промышленности: так, например, фрукты после сублимирования весят в несколько раз меньше, а восстанавливаются в воде. Сублимированные продукты значительно превосходят сушеные по пищевой ценности, так как возгонке поддаётся только вода, а при термическом испарении теряются многие полезные вещества. Недостатком пищевой сублимации является использование заморозки, что приводит к разрушению клеток расширяющейся при замерзании водой.
Реализации эффекта
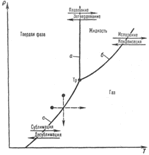
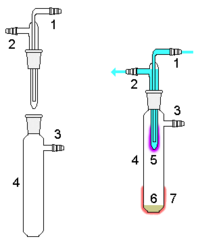
Простой сублимационный аппарат
Рис.1
На рисунке 1 приведен простой сублимационный аппарат. Холодная вода, циркулирующая в конденсаторе, осаждающем на себе пар.
1 – вход холодной воды;
2 – выход холодной воды;
3 – вакуум/газ линия;
4 – сублимационная камера;
5 – сублимируемый продукт;
6 – сырой материал;
7 – внешний нагрев.
Литература
 1. Скворцов А.М.// Обычные и необычные фазовые переходы, 1996, №8, с.103-108.
1. Скворцов А.М.// Обычные и необычные фазовые переходы, 1996, №8, с.103-108.
 2. Пригожин И. От существующего к возникающему. - М.: Наука, 1985.
2. Пригожин И. От существующего к возникающему. - М.: Наука, 1985.
 3. Гиршфельдер Дж., КертиссЧ., Берд Р., Молекулярная теория газов и жидкостей, пер. с англ. - М.: Изд. ин. лит., 1961.
3. Гиршфельдер Дж., КертиссЧ., Берд Р., Молекулярная теория газов и жидкостей, пер. с англ. - М.: Изд. ин. лит., 1961.
 4. Рид Р., ПраусницДж., Шервуд Т., Свойства газов и жидкостей, пер. с англ., - Л.:Наука, 1982.
4. Рид Р., ПраусницДж., Шервуд Т., Свойства газов и жидкостей, пер. с англ., - Л.:Наука, 1982.


![]() 1. Скворцов А.М.// Обычные и необычные фазовые переходы, 1996, №8, с.103-108.
1. Скворцов А.М.// Обычные и необычные фазовые переходы, 1996, №8, с.103-108.
![]() 2. Пригожин И. От существующего к возникающему. - М.: Наука, 1985.
2. Пригожин И. От существующего к возникающему. - М.: Наука, 1985.
![]() 3. Гиршфельдер Дж., КертиссЧ., Берд Р., Молекулярная теория газов и жидкостей, пер. с англ. - М.: Изд. ин. лит., 1961.
3. Гиршфельдер Дж., КертиссЧ., Берд Р., Молекулярная теория газов и жидкостей, пер. с англ. - М.: Изд. ин. лит., 1961.
![]() 4. Рид Р., ПраусницДж., Шервуд Т., Свойства газов и жидкостей, пер. с англ., - Л.:Наука, 1982.
4. Рид Р., ПраусницДж., Шервуд Т., Свойства газов и жидкостей, пер. с англ., - Л.:Наука, 1982.