|
|

 |
|
Межотраслевая Интернет-система поиска и синтеза физических принципов действия преобразователей энергии
|
Общий каталог эффектов
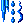 | Плавление |
 |
Переход вещества из кристаллического состояния в жидкое
Описание
Плавление, переход вещества из кристаллического (твердого) состояния в жидкое, происходит с поглощение теплоты (фазовый переход I рода). Главными характеристиками плавления чистых веществ является температура плавления (Тпл) и теплота плавления (Lпл).
Температура плавления зависит от внешнего давления р; на диаграмме состояния чистого вещества эта зависимость изображается кривой плавления (кривой сосуществования твердой и жидкой фаз, AС или AС′ на рис.1).Плавление сплавов и твёрдых растворов происходит, как правило, в интервале температур (исключение составляют эвтектики с постоянной Тпл). Зависимость температуры начала и окончания плавления сплава от его состава при данном давлении изображается на диаграммах состояния специальными линиями (кривые ликвидуса и солидуса. У ряда высокомолекулярных соединений (например, у веществ, способных образовывать жидкие кристаллы) переход из твёрдого кристаллического состояния в изотропное жидкое происходит постадийно (в некотором температурном интервале), каждая стадия характеризует определённый этап разрушения кристаллической структуры.
Диаграмма состояния чистого вещества. Линии AС и AС′ – кривые плавления, по линии AС′ плавятся вещества с аномальным изменением объема при плавлении. Точка А – тройная точка; В – критическая точка
Рис. 1
Наличие определённой температуры плавления – важный признак правильного кристаллического строения твёрдых тел. По этому признаку их легко отличить от аморфных твёрдых тел, которые не имеют фиксированной Тпл. Аморфные твёрдые тела переходят в жидкое состояние постепенно, размягчаясь при повышении температуры.
Самую высокую температуру плавления среди чистых металлов имеет вольфрам (3410 °С), самую низкую – ртуть (–38,9 °С). К особо тугоплавким соединениям относятся: TiN (3200 °С), HfN (3580 °С), ZrC (3805 °С), TaC (4070 °С), HfC (4160 °С) и др. Как правило, для веществ с высокой Тпл характерны более высокие значения Qпл. Примеси, присутствующие в кристаллических веществах, снижают их Тпл. Этим пользуются на практике для получения сплавов с низкой Тпл и охлаждающих смесей.
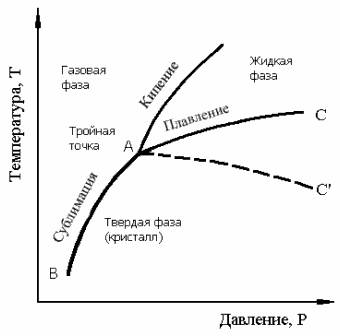
Плавление начинается при достижении кристаллическим веществом Тпл. С начала плавления до его завершения температура вещества остаётся постоянной и равной Тпл, несмотря на сообщение веществу теплоты (рис.2). Нагреть кристалл до Т > Тпл в обычных условиях не удаётся, тогда как при кристаллизации сравнительно легко достигается значительное переохлаждение расплава.
Остановка температуры при плавлении кристаллического тела. По оси абсцисс отложено время t, пропорциональное равномерно подводимому к телу количеству теплоты.
Рис. 2
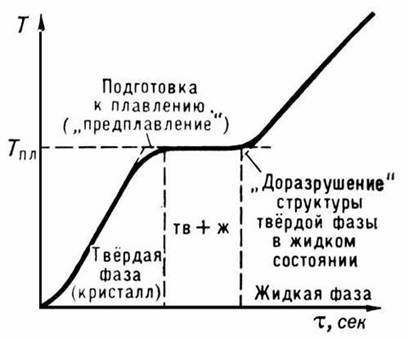
Характер зависимости Тпл от давления р определяется направлением объёмных изменений (ΔVпл) при плавлении. В большинстве случаев плавление вещества сопровождается увеличением их объёма (обычно на несколько %). Если это имеет место, то возрастание давления приводит к повышению Тпл (рис.3). Однако у некоторых веществ (воды, ряда металлов и металлидов, см. рис.1) при плавлении происходит уменьшение объёма. Температура плавления этих веществ при увеличении давления снижается.
Изменение температуры плавления Тпл (°С) щелочных металлов с увеличением давления p (кбар). Кривая плавления Cs указывает на существование у него при высоких давлениях двух полиморфных превращений (а и в).
Рис. 3
Плавление сопровождается изменением физических свойств вещества: увеличением энтропии, что отражает разупорядочение кристаллической структуры вещества; ростом теплоёмкости, электрического сопротивления [исключение составляют некоторые полуметаллы (Bi, Sb) и полупроводники (Ge), в жидком состоянии обладающие более высокой электропроводностью]. Практически до нуля падает при плавлении сопротивление сдвигу (в расплаве не могут распространяться поперечные упругие волны), уменьшается скорость распространения звука (продольных волн) и т.д.
Согласно молекулярно-кинетическим представлениям, плавление осуществляется следующим образом. При подведении к кристаллическому телу теплоты увеличивается энергия колебаний (амплитуда колебаний) его атомов, что приводит к повышению температуры тела и способствует образованию в кристалле различного рода дефектов (незаполненных узлов кристаллической решётки – вакансий; нарушений периодичности решётки атомами, внедрившимися между её узлами, и др). В молекулярных кристаллах может происходить частичное разупорядочение взаимной ориентации осей молекул, если молекулы не обладают сферической формой. Постепенный рост числа дефектов и их объединение характеризуют стадию предплавления. С достижением Тпл в кристалле создаётся критическая концентрация дефектов, начинается плавление – кристаллическая решётка распадается на легкоподвижные субмикроскопические области. Подводимая при плавлении теплота идёт не на нагрев тела, а на разрыв межатомных связей и разрушение дальнего порядка в кристаллах. В самих же субмикроскопических областях ближний порядок в расположении атомов при плавлении существенно не меняется (координационное число расплава при Тпл в большинстве случаев остаётся тем же, что и у кристалла). Этим объясняются меньшие значения теплот плавления Qпл по сравнению с теплотами парообразования и сравнительно небольшое изменение ряда физических свойств веществ при их плавлении.
Плавление занимает особое положение в общей системе фазовых переходов как универсальное физическое явление, которое может быть обнаружено практически у всех веществ. В этом отношении плавление можно сравнить только с кипением, которое столь же универсально. Более существенна еще одна особенность плавления, на этот раз не имеющая аналогов, заключающаяся в том, что плавление представляет собой результат конкуренции между двумя конденсированными и вместе с тем принципиально различными состояниями вещества: жидкостью и твердым телом. Совершенно естественно, что это явление не могло не привлечь внимания. В результате кропотливой работы многих исследователей сейчас накоплено большое количество экспериментальных фактов и эмпирических обобщений, касающихся плавления и кристаллизации. Тем не менее все обилие экспериментального материала пока еще мало способствовало созданию сколько-нибудь приемлемой теории плавления, которая могла бы объединить уже известные факты и предсказать какие-либо новые стороны явления. Если не рассматривать известных трудностей строгого статистического подхода к проблеме фазового перехода вообще, то подобная ситуация связана прежде всего с отсутствием достаточно пригодных моделей жидкого состояния, качественно верно отражающих реальность.
Ключевые слова
Разделы наук
Применение эффекта
Процесс плавления играет важную роль в природе (плавление снега и льда на поверхности Земли, плавление минералов в её недрах и т.д.) и в технике (производство металлов и сплавов, литьё в формы и др.).
Працесс плавления играют важную роль прежде всего в процессах сварки и пайки.
Сварка плавлением осуществляется нагревом свариваемых кромок до температуры плавления без сдавливания свариваемых деталей.
При нагреве с повышением температуры снижается твёрдость металла и возрастает его пластичность. Металл, твёрдый и малопластичный при комнатной температуре, при достаточном нагреве может стать очень мягким и пластичным. Дальнейшим повышением температуры можно довести металл до расплавления; в этом случае отпадают все затруднения, связанные с твёрдостью металла; объёмы жидкого металла самопроизвольно сливаются в общую сварочную ванну.
Во многих случаях на процесс сварки существенно влияют загрязнения поверхности металла: преимущественно окислы и жировые плёнки. Эти загрязнения, попадая в сварное соединение, могут снижать качество сварки. Они, в отличие от адсорбированных газов, могут быть удалены с поверхности металла механически (щётками, абразивами и т.д.) или химически (растворителями, травителями, и флюсами).
Реализации эффекта
У сплавов, как правило, нет определённой температуры плавления; процесс их плавления происходит в конечном диапазоне температур. На диаграммах состояния «температура – относительная концентрация» имеется конечная область сосуществования жидкого и твёрдого состояния, ограниченная кривыми ликвидуса и солидуса. Аналогичная ситуация имеет место и в случае многих твёрдых растворов.
Фиксированной температуры плавления нет также у аморфных тел; они переходят в жидкое состояние постепенно, размягчаясь при повышении температуры.
Кинетика плавления
Поясним вначале, почему при некоторой температуре тело предпочитает разорвать часть межатомных связей и из упорядоченного состояния (кристалл) перейти в неупорядоченное (жидкость).
Как известно из термодинамики, при фиксированной температуре тело стремится минимизировать свободную энергию F = E – TS. При низких температурах второе слагаемое (произведение температуры и энтропии) несущественно, и в результате всё сводится к минимизации обычной энергии E. Состояние с минимальной энергией – это кристаллическое твёрдое тело. При повышении температуры, второе слагаемое становится всё важнее, и при некоторой температуре оказывается выгоднее разорвать некоторые связи. При этом обычная энергия E слегка повысится, но при этом сильно возрастет и энтропия, что в результате приведёт к понижению свободной энергии.
Динамика плавления
В динамике, плавление происходит следующим образом. При повышении температуры тела увеличивается амплитуда тепловых колебаний его молекул, и время от времени возникают дефекты решетки. Каждый такой дефект требует определённого количества энергии, поскольку он сопровождается разрывом некоторых межатомных связей. Стадия рождения и накопления дефектов называется стадией предплавления. Кроме того, на этой стадии, как правило, возникает квази-жидкий слой на поверхности тела. При некоторой температуре концентрация дефектов становится столь большой, что приводит к потере ориентационного порядка в образце.
Плавление в двумерных системах
В двумерных или квази-двумерных системах кристалл является гораздо более шатким объектом, чем в трёхмерном случае, а именно у двумерного кристалла нет дальнего позиционного порядка. (Для сравнения: в одномерном случае кристалл при конечной температуре вообще не может быть стабильным!) Как выяснилось, это приводит к тому, что плавление двумерного кристалла происходит в два этапа. Вначале кристалл переходит в так называемую гексатическую фазу, в которой теряется ближний позиционный порядок, но сохраняется ориентационный, а затем происходит потеря и ориентационного порядка и тело становится жидким.
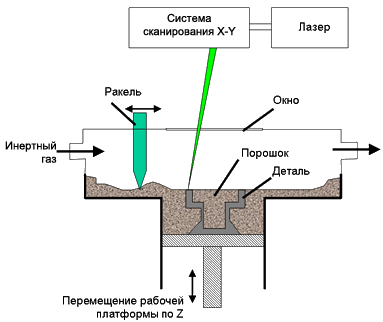
Селективное лазерное плавление металлического порошка (SLM) подходит для изготовления комплексных инструментов и элементов конструкции (деталей, узлов), причем в сравнении с обычными методами изготовления преимущество по издержкам и времени в настоящее время может достигать 30%. Точность от 0,01 мм, как при обычном изготовлении форм ручным или CNC/EDM методами.
Рис. 1
Литература
 1. Френкель Я. И., Кинетическая теория жидкостей, Собр. избр. трудов, т. 3, М. —Л., 1959.
1. Френкель Я. И., Кинетическая теория жидкостей, Собр. избр. трудов, т. 3, М. —Л., 1959.
 2. Данилов В. И., Строение и кристаллизация жидкости, К., 1956.
2. Данилов В. И., Строение и кристаллизация жидкости, К., 1956.
 3. Глазов В. М., Чижевская С. Н., Глаголева Н. Н., Жидкие полупроводники, М., 1967.
3. Глазов В. М., Чижевская С. Н., Глаголева Н. Н., Жидкие полупроводники, М., 1967.
 4. Уббелоде А., Плавление и кристаллическая структура, пер. с англ., М., 1969.
4. Уббелоде А., Плавление и кристаллическая структура, пер. с англ., М., 1969.


![]() 1. Френкель Я. И., Кинетическая теория жидкостей, Собр. избр. трудов, т. 3, М. —Л., 1959.
1. Френкель Я. И., Кинетическая теория жидкостей, Собр. избр. трудов, т. 3, М. —Л., 1959.
![]() 2. Данилов В. И., Строение и кристаллизация жидкости, К., 1956.
2. Данилов В. И., Строение и кристаллизация жидкости, К., 1956.
![]() 3. Глазов В. М., Чижевская С. Н., Глаголева Н. Н., Жидкие полупроводники, М., 1967.
3. Глазов В. М., Чижевская С. Н., Глаголева Н. Н., Жидкие полупроводники, М., 1967.
![]() 4. Уббелоде А., Плавление и кристаллическая структура, пер. с англ., М., 1969.
4. Уббелоде А., Плавление и кристаллическая структура, пер. с англ., М., 1969.