|
|

 |
|
Межотраслевая Интернет-система поиска и синтеза физических принципов действия преобразователей энергии
|
Общий каталог эффектов
 | Изохорный процесс |
 |
Процесс изменения давления идеального газа в зависимости от его температуры при постоянном объеме
Анимация
Описание
Изохорный процесс (изохорический процесс) (от греческого isos – равный, одинаковый и chora – пространство) – термодинамический процесс, происходящий в системе при постоянном объёме p=const*(T), где p-давление, T-температура, а константа пропорциональна количеству вещества и обратно пропорциональна объему газа. На термодинамической диаграмме изохорный процесс изображается изохорой.
Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным.
Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или
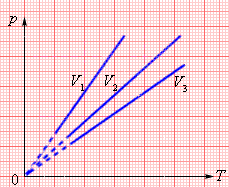
На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур (рисунок 1).
Семейство изохор на плоскости (p, T) V3 > V2 > V1.
Рис.1
Экспериментально зависимость давления газа от температуры исследовал французский физик Ж. Шарль (1787 г.). Поэтому уравнение изохорного процесса называется законом Шарля.
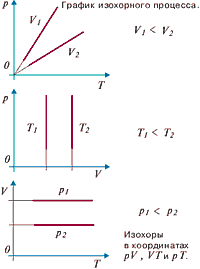
Диаграммы изохорного процесса
Рис.2
Ключевые слова
Разделы наук
Используется в научно-технических эффектах
Используется в областях техники и экономики
Используются в научно-технических эффектах совместно с данным эффектом естественнонаучные эффекты
Применение эффекта
Изохорный процесс осуществляется в газах и жидкостях, находящихся в замкнутом сосуде с неизменным объёмом. При изохорном процессе система не совершает работы и подведённая те-плота dQ целиком расходуется на изменение внутренней энергии: dU=dQ, следовательно. dQ=Cvd,T; Сv= = (dU/dT)v – теплоёмкость при постоянном объёме, которая всегда меньше теплоёмкости при постоянном давлении. В идеальном газе при изохорном процессе давление пропорционально температуре {Марля закон). Для неидеального газа закон Шарля не справедлив, т. к. часть сообщённой газу теплоты идет на увеличение энергии взаимодействия частиц. Изменение энтропии при изохорном процессе равно
Реализации эффекта
Холодильные процессы обеспечивают непрерывное искусств, охлаждение различных веществ (тел) путем отвода от них теплоты. Естественное охлаждение с помощью холодной воды или воздуха позволяет охладить вещество до температуры охлаждающей среды и не требует подвода энергии. Охлаждение до более низких температур происходит в искусственных холодных средах, на создание которых расходуется механическая, тепловая или химическая энергия. Охлаждение до температур выше 120 К принято наз. умеренным, ниже – глубоким или криогенным.
Искусственные холодные среды. Для их получения необходим перенос теплоты с низкого на более высокий температурный уровень, которым, как правило, является температура окружающей среды. Этот перенос осуществляется с использованием т. наз. обратимых круговых термодинамических циклов, которые в промышленности обычно реализуются в холодильных установках. В последних холодная среда создается с помощью рабочих тел, наз. холодильными агентами или просто хладагентами (вода, NH3, пропан-пропиленовые смеси, хладоны, сжиженные газы - воздух, N2, Н2, Не и др.).
В лабораторной практике холодные среды получают, приготовляя т. наз. охлаждающие смеси- системы из двух или несколько твердых (либо твердых и жидких) веществ, при смешении которых вследствие поглощения теплоты при плавлении или растворении происходит понижение температуры. Наиболее употребительны смеси из льда и NaCl, твердого СО2 и этанола (-77 °С) и др. Для достижения криогенных температур в лабораториях применяют сжиженные газы, напр. N2.
Термодинамические основы получения холода. Согласно второму началу термодинамики, указанный выше перенос теплоты самопроизвольно не происходит, требуя затрат работы. В термодинамических процессах подвод или отвод теплоты q описывается через изменение энтропии dS системы: dq = TdS, где Т - температура. Отсюда следует, что при подводе к телу теплоты его энтропия возрастает, а при отводе теплоты - уменьшается. В непрерывных X. п. хладагент должен принять теплоту от охлаждаемого тела на нижнем температурном уровне, отдать теплоту на верх. уровне к.-л. теплоприемнику и вернуться в исходное состояние. Поэтому в установившемся процессе суммарная энтропия хладагента не изменяется (dS=0). Поскольку при передаче теплоты от охлаждаемого тела энтропия хладагента повышается, в любой холодильной установке должен проходить иной (компенсирующий) процесс, при котором энтропия хладагента уменьшается. В общем случае энтропия м. б. представлена как функция температуры и к.-л. другого параметра тела (напр., давление, фазовое состояние, степень намагниченности). Поэтому, если имеется изотермический или близкий к нему процесс, в котором наблюдается значит. изменение энтропии при изменении иного параметра, то подобный процесс можно рассматривать как потенциальную основу для создания холодильных установок. К таким процессам относятся, напр., изотермические процессы сжатия либо адсорбции газов, намагничивания парамагнетиков и сверхпроводников. При этом низкая температура достигается соотв. в адиабатических процессах расширения и десорбции газов, размагничивания парамагнетиков и сверхпроводников.
Перечисленные и иные процессы искусств. охлаждения в большинстве случаев осуществляются: 1) путем теплообмена между охлаждаемыми веществами и хладагентами – испаряющимися низкокипящими жидкостями, температура которых за счет уменьшения энтальпии i понижается до температуры кипения при давлении испарения; 2) изоэнтальпийным (i = const) расширением газов, предварительно сжатых в компрессорах, или жидкостей при их прохождении через сужение (вентиль, кран, пористая перегородка), т. е. их дросселированием (процесс протекает адиабатически без совершения внеш. работы) с использованием эффекта Джоуля – Томсона, или дроссельного эффекта, – отрицательные либо положительные изменения температуры тела при отсутствии подвода к телу или отвода от него теплоты; 3) адиабатическим (изоэнтропийным, S = const) расширением газов с совершением внеш. работы в т. наз. детандерах - машинах, устроенных подобно поршневому компрессору или турбокомпрессору; 4) сочетанием обоих методов расширения. Эти и другие методы получения холода рассмотрены ниже.
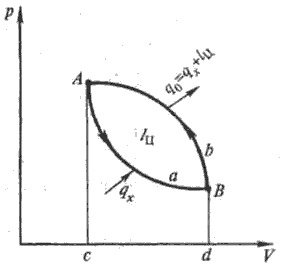
Принцип работы холодильных установок. Его удобно иллюстрировать с помощью идеального (воображаемого) холодильного процесса (цикла) в координатах р - V (рисунок 1; р, V- давление в системе и ее объем). При сжатии в компрессоре (процесс ВbА)рабочего тела его температура Т повышается; при этом в окружающую среду с т-рой Т0 передается удельная (на единицу кол-ва хладагента) теплота q0 (площадь AbBdcA) и энтропия рабочего тела понижается; в конце сжатия Т = Т0. При послед. расширении (процесс АаВ)хладагента его температура понижается. Затем к нему от охлаждаемой среды переносится теплота qx (площадь AaBdcA)и энтропия рабочего тела возрастает.
Повторяя указанные процессы, получают непрерывный круговой холодильный цикл с постоянной холодопроизводительностью qx (кол-во теплоты, отнимаемой от охлаждаемого тела). Расходуемая в цикле механическая работа lц (площадь АаВbА), параметры q0 и qx по закону сохранения энергии связаны между собой выражением: q0 = qx + lц. Энергетические показатели цикла характеризуются т. наз. холодильным коэффициентом ε = qx/lц.
Идеальный холодильный цикл
Рис.1
Литература
 1. Прохоров А.М Физическая энциклопедия М.: Большая Российская энциклопедия. Т.1., 1994
1. Прохоров А.М Физическая энциклопедия М.: Большая Российская энциклопедия. Т.1., 1994
 2. Фриш С.Э., Тиморева А.В. Курс общей физики. Физические основы механики. Молекулярная физика. Колебания и волны. т. 1. М.:1962
2. Фриш С.Э., Тиморева А.В. Курс общей физики. Физические основы механики. Молекулярная физика. Колебания и волны. т. 1. М.:1962
 3. Рейф Ф. Берклеевский курс лекций: статистическая физика (Том 5), 1965
3. Рейф Ф. Берклеевский курс лекций: статистическая физика (Том 5), 1965


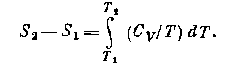
![]() 1. Прохоров А.М Физическая энциклопедия М.: Большая Российская энциклопедия. Т.1., 1994
1. Прохоров А.М Физическая энциклопедия М.: Большая Российская энциклопедия. Т.1., 1994
![]() 2. Фриш С.Э., Тиморева А.В. Курс общей физики. Физические основы механики. Молекулярная физика. Колебания и волны. т. 1. М.:1962
2. Фриш С.Э., Тиморева А.В. Курс общей физики. Физические основы механики. Молекулярная физика. Колебания и волны. т. 1. М.:1962
![]() 3. Рейф Ф. Берклеевский курс лекций: статистическая физика (Том 5), 1965
3. Рейф Ф. Берклеевский курс лекций: статистическая физика (Том 5), 1965